1 lít dung dịch CH3COOH 0,01M có chứa tổng số 6,28.1021 ion và phân tử CH3COOH. Tính độ điện li của axit này?

Những câu hỏi liên quan
Trong 2 lít dung dịch CH3COOH 0,01M có 12,522.1021 phân tử và ion. Phần trăm số phân tử axit CH3COOH phân li thành ion là:
A. 0,99%
B. 1,98%
C. 2,96%
D. 3,95%
Đáp án D
Số mol CH3COOH ban đầu là 0,01.2=0,02 mol
Tổng số mol phân tử và ion sau khi phân li là: (12,522.1021)/ (6,023.1023)=0,02079 mol
![]()
Ban đầu 0,02 mol
Phản ứng x x x mol
Sau 0,02-x x x mol
Tổng số mol sau phân li là: 0,02-x+ x+ x=0,02079 mol suy ra x=7,9.10-4 mol
Số phân tử CH3COOH phân li ra ion là 7,9.10-4.100%/ 0,02=3,95%
Đúng 0
Bình luận (0)
Cho 2 dung dịch HCl và CH3COOH có cùng nồng độ. Dung dịch HCl có pH x, dung dịch CH3COOH có pH y. Bỏ qua sự điện li của nước, các dung dịch ở cùng nhiệt độ phòng. Biết ở nhiệt độ phòng, cứ 100 phân tử CH3COOH thì có 1 phân tử phân li ra ion. Mối liên hệ của x và y là: A. x y - 2 B. y x – 2 C. x 2y D. y 2x
Đọc tiếp
Cho 2 dung dịch HCl và CH3COOH có cùng nồng độ. Dung dịch HCl có pH = x, dung dịch CH3COOH có pH = y. Bỏ qua sự điện li của nước, các dung dịch ở cùng nhiệt độ phòng. Biết ở nhiệt độ phòng, cứ 100 phân tử CH3COOH thì có 1 phân tử phân li ra ion. Mối liên hệ của x và y là:
A. x = y - 2
B. y = x – 2
C. x = 2y
D. y = 2x
Không mất tính tổng quát, ta đặt:
![]()
Vì HCl là chất điện li mạnh nên ta có phương trình điện li như sau:
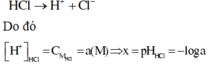
Vì CH3COOH là chất điện li yếu nên ta có phương trình điện li như sau
Xét cân bằng điện li: CH3COOH ⇌ CH3COO- + H+
Nồng độ ban đầu: aM 0
Nồng độ phân li: 0,01a M → 0,01a M
Nồng độ cân bằng: 0,99a M 0,01a M
Ta có
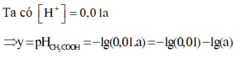
![]()
Đáp án A.
Đúng 0
Bình luận (0)
Trong dung dịch CH3COOH 4,3.
10
-
2
M, người ta xác định được nồng độ
H
+
bằng
8
,
6
.
10
-
4
mol/l. Hỏi có bao nhiêu phần trăm phân tử
C
H
3
C
O
O
H
trong dung dịc...
Đọc tiếp
Trong dung dịch CH3COOH 4,3. 10 - 2 M, người ta xác định được nồng độ H + bằng 8 , 6 . 10 - 4 mol/l. Hỏi có bao nhiêu phần trăm phân tử C H 3 C O O H trong dung dịch này điện li ra ion ?
Dung dịch HCl và dung dịch CH3COOH có cùng nồng độ mol/lít. Giá trị pH tương ứng của dịch tương ứng là x và y. Quan hệ giữa x và y là ( giả thiết cứ 100 phân tử 2 dung CH3COOH thì có 1 phân tử điện li) A. y 100x B. y 2x C. y x-2 D. y x+2
Đọc tiếp
Dung dịch HCl và dung dịch CH3COOH có cùng nồng độ mol/lít. Giá trị pH tương ứng của dịch tương ứng là x và y. Quan hệ giữa x và y là ( giả thiết cứ 100 phân tử 2 dung CH3COOH thì có 1 phân tử điện li)
A. y = 100x
B. y = 2x
C. y = x-2
D. y = x+2
Đáp án D
HCl → H++ Cl-
[H+] = a M ; suy pH = -log a = x
![]()
Cứ 100 phân tử CH3COOH thì có 1 phân tử điện li nên [H+] = a/100 M suy ra pH = -log (a/100) = y
Do đó y-x = 2
Đúng 0
Bình luận (0)
Dung dịch HCl và CH3COOH có cùng nồng độ. pH của hai dung dịch này tương ứng là x và y. Cứ 100 phân tử CH3COOH thì có 1 phân tử phân li. Quan hệ giữa x và y là: A. y 100x B. y 2x C. y x – 2 D. y x + 2
Đọc tiếp
Dung dịch HCl và CH3COOH có cùng nồng độ. pH của hai dung dịch này tương ứng là x và y. Cứ 100 phân tử CH3COOH thì có 1 phân tử phân li. Quan hệ giữa x và y là:
A. y = 100x
B. y = 2x
C. y = x – 2
D. y = x + 2
Đáp án D
Cứ 100 phân tử CH3COOH thì có 1 phân tử phân li
⇒ nH+/HCl = 100nH+/ CH3COOH
Mà dung dịch HCl và CH3COOH có cùng nồng độ
⇒ [H+/HCl] = 100[H+/ CH3COOH]
⇒ -log[H+/HCl] = -2 - log[H+/ CH3COOH]
⇒ x = -2 + y ⇒ y = x + 2
Đáp án D.
Đúng 0
Bình luận (0)
Xét dung dịch axit yếu CH3COOH 0,01M . Không kể đến sự điện li của nước,giá trị của độ pH
ta có : 0,01>4,47.10-7=>[H+]=0,01=> pH = -log(H+)
=> pH = -log(0,01) = 2
:)
Đúng 0
Bình luận (0)
Trong dung dịch CH 3 COOH 0,043M, cứ 100 phân tử hòa tan có 2 phân tử phân li thành ion. Nồng độ của ion H+ là
A. 0,001M.
B. 0,086M.
C. 0,00086M.
D. 0,043M
Dung dịch có chứa CH3COOH 0,1M và CH3COONa 0,1M. Tính độ pH của dung dịch. Biết rằng hằng số axit của CH3COOH là Ka 10-4,76.
Đọc tiếp
Dung dịch có chứa CH3COOH 0,1M và CH3COONa 0,1M. Tính độ pH của dung dịch. Biết rằng hằng số axit của CH3COOH là Ka = 10-4,76.
Sửa đề bài Vì CH3COONa là chất điện li mạnh nên được viết trước để tạo môi trường cho cân bằng của chất điện li yếu phân li và cân bằng:
CH³COOH ⇔ CH³COO -+H+
Ban đầu 0,1 0. 0
Phân li xM x. x
Cân bằng 0,1-x 0,1+x x
Suy ra K = \(\dfrac{x(x+0,1)}{0,1-x}\) = 1,8.10 mũ âm ⁵
⇒ x = 1,8 . 10 mũ âm ⁵
⇒pH = log x = 1745
Đúng 0
Bình luận (0)
Cho dd CH3COOH nồng độ 0,043 M . Độ điện li = 0,02
a; dung dịch axit acitic có những phân tử điện li nào
b: tính nồng độ của các chất ion có trong phân tử
Giải
a) Cái này mình không chắc lắm: trong dd CH3COOH có 2 phẩn tử điện li là: CH3COOH và H2O
b)Nồng độ 0,043M chính là nồng độ ban đầu
Ta có công thức \(\alpha\)=[điện li]/[ban đầu]
<=>0,02=[điện li]/0,043<=>[điện li]CH3COOH=8,6.10-4 (M)
Áp dụng phương pháp 3 dòng:
CH3COOH \(\leftrightarrow\) CH3COO- + H+
Bđ:0,043 ----------------0------------------0
Đl:8,6.10-4---------------8,6.10-4------------8,6.10-4
SĐl:0,043-8,6.10-4-------8,6.10-4------------8,6.10-4
Nồng độ các chất và ion sau điện li:
[H+]=[CH3COO-]=8,6.10-4M
Đúng 0
Bình luận (1)
E có thể tham khảo thêm các dạng bài tập như thế này ở đây
https://hoc24.vn/ly-thuyet/gia-tri-ph-cua-cac-dung-dich-axit-bazo.4749/
Đúng 0
Bình luận (2)












